¿Se imaginan ustedes una molécula que según el producto al que se adicione pueda tener un efecto antioxidante o el diametralmente opuesto convirtiéndose en un poderoso agente prooxidante? Pues bien, ese compuesto simpar existe, campa por sus anchas por mi laboratorio y, además, lo pueden ver ustedes cada vez que entren a Scientia porque forma parte de la imagen que identifica a este blog…mi querida ciclodextrina.
La estructura, propiedades y aplicaciones de esta molécula, formada por un grupo de moléculas de glucosa unidas por enlaces α-1-4-glucosídicos y que se puede obtener de forma natural mediante la acción de enzimas microbianas, ya fueron descritas en un post previo acerca de “La reina de la encapsulación molecular” y no vamos a volver a repetirlas.
Sin embargo, hoy vamos a intentar explicar, a través de este grupo de moléculas de carácter glucídico, como gran parte de los errores que se están cometiendo en el área de la investigación bioquímica, y por qué no decirlo también en otros campos, son debidos a las generalizaciones que se suelen hacer sobre las propiedades de un compuesto sean cuales sean las condiciones en las que actúe.
Uno de los sectores de la investigación científica donde mayor número de disparates se están publicando es el campo de las moléculas antioxidantes, lo que ha llevado a que podamos encontrar en la literatura todo tipo de datos contradictorios acerca de la capacidad antioxidante de un compuesto.
A pesar de que las razones de este caos son muchas y de diversa índole, hay dos que destacan por encima de todas. La primera de ellas es el mal uso que se está realizando de las técnicas de medida de la capacidad antioxidante, mezclando conceptos y empleando indistintamente diferentes metodologías como el ORAC, ABTS, FRAP, etc. lo que ha provocado que según sea la técnica empleada se publique que un producto tenga más capacidad antioxidante que otro o justo al revés… y esto no es razonable.
La segunda de las razones que es necesaria aclarar para conocer el comportamiento antiooxidante o prooxidante de una molécula es determinar cuál es su verdadero mecanismo de actuación… y eso es lo que vamos a hacer hoy con un ejemplo realmente llamativo.
Uno de los principales problemas de la industria alimentaria es la rápida degradación del color de determinadas frutas y verduras a la hora de su procesado para la elaboración de distintos productos como zumos, néctares, etc.
Debido a ello, y a que la mejora del perfil sensorial de los alimentos es uno de los grandes objetivos de la industria alimentaria, la búsqueda de nuevas sustancias con alto valor añadido que le confieran a los alimentos un elevado valor nutricional y organoléptico es un importante reto este sector.
Y como el autor de este blog se mete en todos los charcos allá que fui, con mis ciclodextrinas en mano, a sacar a mi querida industria alimentaria del problema del deterioro de sus zumos de frutas debido a su oscurecimiento prematuro… para que luego se queje este sector de que soy su «martillo pilón»… que también.
Sin embargo tengo que reconocer que la tarea no fue nada fácil. Pasado algún tiempo puedo asegurar que los resultados que encontré investigando el efecto de la adición de estas moléculas encapsulantes a diferentes zumos de frutas constituyeron el caso más inesperado y sorprendente que me he encontrado en los años que llevo metido en el laboratorio… que ya son muchos.
Las ciclodextrinas, esos agentes con forma de tronco cónico y cuya propiedad más importante es su capacidad para incluir una amplia variedad de moléculas orgánicas e inorgánicas, comúnmente denominadas moléculas huésped, dentro de su cavidad hidrofóbica, tenían un comportamiento totalmente opuesto, antioxidante y prooxidante, según el zumo al que se adicionaran… ¿y eso por qué?
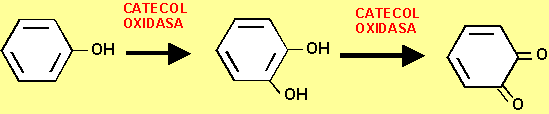
La reacción bioquímica responsable del oscurecimiento de zumos de frutas se conoce como pardeamiento enzimático.
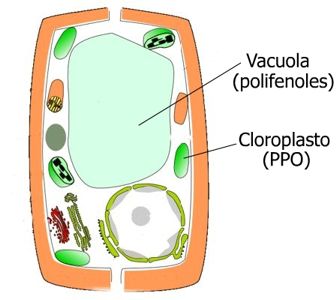
Esta reacción es llevada a cabo, en sus dos primeras etapas, por una enzima llamada polifenoloxidasa (también conocida por catecol oxidasa) que se encuentra generalmente en los cloroplastos de las células vegetales la cual, a través de dos pasos, convierte los monofenoles presentes en las vacuolas de dichas células en difenoles y, posteriormente, oxida estos difenoles a ortoquinonas. Finalmente, y a través de una reacción química, estas quinonas se convierten en esas manchas oscuras (melaninas) que todos hemos visto en manzanas, patatas, peras, etc.
En circunstancias normales los polifenoles no tienen contacto con la enzima y la reacción no se produce a velocidad apreciable, pero si por un impacto u otro procedimiento similar (al pelar con un cuchillo) se produce la ruptura de los compartimentos en que ambos productos se alojan, éstos se ponen en contacto y la producción de quinonas comienza.
Pues bien, según la hipótesis que se planteó antes de llevar a cabo nuestros experimentos, la adición de ciclodextrinas a los zumos de frutas podría dar lugar a que debido a la naturaleza hidrofóbica de muchos de los fenoles presentes en las frutas anteriormente citadas, éstos fuesen encapsulados en el interior de la cavidad hidrofóbica de las ciclodextrinas y así la enzima polifenoloxidasa no tuviese acceso a ellos provocando que el color original del zumo se mantuviese más tiempo.
Una vez realizados los pertinentes ensayos en zumos procedentes de diversas frutas la teoría se confirmó. En el caso de los zumos de pera, melocotón, manzana y uva, las ciclodextrinas ralentizaron la degradación de color gracias a la microencapsulación de los fenoles presentes en esas frutas en el interior de las mismas.
En la figura adjunta se puede observar el efecto de la adición de distintas concentraciones de un tipo de ciclodextrina al zumo de manzana durante los primeros 60 minutos de su procesado. Como se puede apreciar, elevadas concentraciones del agente encapsulante llegan a ralentizar drásticamente la evolución de la variación total de color del zumo de manzana (∆E), parámetro íntimamente relacionado con la degradación del color en este tipo de zumos.
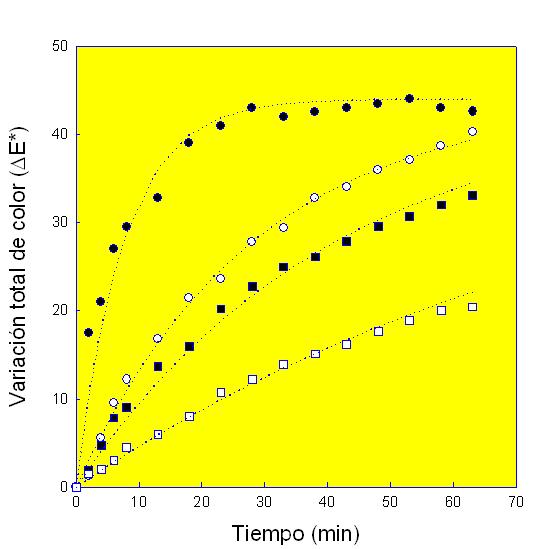
Efecto de la adición de distintas concentraciones de maltosyl-B-CD sobre ΔE* del zumo de manzana a 25ºC. no maltosy-B-CD (●); 30 mM (○), 60 mM (■) and 90 mM (□)
Según el efecto observado, y que podemos apreciar “in vivo” para el caso del zumo de pera en la siguiente fotografía, la ciclodextrina se comporta como un “antioxidante aparente”. Sin embargo, y a pesar de que el efecto final es similar al que se puede observar cuando se emplea un antioxidante real como es el caso del ácido ascórbico, el mecanismo de actuación es diferente.
Mientras el ácido ascórbico ejerce un papel reductor inhibiendo temporalmente la oxidación de difenoles a quinonas, las ciclodextrinas encapsulan los fenoles dificultando la actuación de la enzima… si lo leen dos veces verán que no es tan complicado entenderlo.
Cuando parecía que el sistema estaba controlado, y habíamos encontrado al antioxidante “natural” ideal, la sorpresa saltó en el laboratorio. Empleando el plátano como fuente vegetal pudimos observar como la adición de ciclodextrinas no solamente no disminuía el grado de pardeamiento sino que, sorprendentemente, lo aumentó.
La ciclodextrina se comportaba como un agente prooxidante… justo lo contrario que habíamos publicado con el zumo pera, manzana, uva o melocotón donde eran antioxidantes…. la solución, como casi siempre, estaba en la bibliografía.
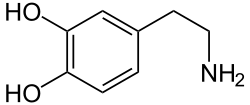
La búsqueda bibliográfica se centró en encontrar cuales eran los sustratos fenólicos presentes en el plátano susceptibles de ser oxidados por polifenoloxidasa y que diesen lugar al oscurecimiento del plátano. La dopamina fue la respuesta. Esta catecolamina es oxidada en el plátano por nuestra enzima para dar un compuesto que, a menudo, es rechazado por el consumidor…. ¿pero qué característica tiene la dopamina que la diferencia del resto de sustratos fenólicos que podemos encontrar en otras fuentes vegetales y que provoca que las ciclodextrinas no se comporten como antioxidantes sino como prooxidantes?
Como pueden observar en la figura adjunta la dopamina es un compuesto eminentemente hidrofílico, contrariamente a lo que ocurre en la pera, uva, manzana o melocotón donde los principales fenoles presentes (acido clorogénico, ácido cafeico, catequina, epicatequina) poseen una importante naturaleza hidrofóbica… y es esta particularidad de la dopamina la que le impide que pueda entrar en la cavidad interna de las ciclodextrinas… y por ello la enzima polifenoloxidasa no tiene ninguna dificultad para provocar el oscurecimiento del zumo de plátano.
Sin embargo, y si están siguiendo correctamente el hilo de este post, una pregunta debería asaltarles. Debido al carácter hidrofílico de la dopamina estaría justificado que la adición de ciclodextrinas no tenga efecto alguno sobre el pardeamiento enzimático… pero esto no justifica que la presencia de las mismas provoque que los zumos de plátano a los que se adicionan estos agentes encapsulantes estén aun más oscuros que los que no las llevan… la solución, de nuevo, estaba en la bibliografía.
Estudiando la composición bromatológica del plátano resulta que esta fruta posee en su estructura dos potentes inhibidores de la enzima responsable de su pardeamiento y que mantienen al plátano verde durante más tiempo.
Pues bien, esos dos inhibidores de la polifenoloxidasa son de carácter hidrofóbico y, tras varios ensayos en el laboratorio, observamos que eran capaces de ser encapsulados en las ciclodextrinas… por lo que no podían llevar a cabo su acción contra el pardemiento del plátano en presencia de estos agentes encapsulantes.
Al desactivar las ciclodextrinas el mecanismo de actuación de estos inhibidores de polifenoloxidasa, la enzima podía dar rienda suelta a su mecanismo oxidante con mayor facilidad que si no hubieran encapsulantes en el medio… y el zumo de plátano se ponía negro en cuestión de segundos.
Con esto hemos demostrado la razón por la cual las reinas de la encapsulación molecular, las ciclodextrinas, producen en el plátano el efecto contrario al observado en la mayoría de los zumos de futas comportándose como auténticos prooxidantes. Por una parte no pueden encapsular a la dopamina, el sustrato mayoritario de polifenoloxidasa presente en el plátano y, por otra, encapsulan a los inhibidores naturales de esta enzima desactivando su mecanismo de actuación y disparando el pardeamiento enzimático.
Todo lo expuesto en el post de hoy, donde se demuestra como el uso de ciclodextrinas como una nueva tecnología que ralentiza el pardeamiento enzimático debe ser evaluado para el caso de cada alimento, ya que dependiendo del tipo de fenoles que se encuentren en su estructura el efecto puede ser positivo o negativo, nos lleva a tres conclusiones principales.
La primera de ellas es que la investigación básica y la aplicada deben ir siempre de la mano. El conocimiento del mecanismo de actuación a nivel molecular de un compuesto es absolutamente necesario si luego queremos usarlo en el sector industrial.
Por otra parte, los resultados expuestos en esta entrada muestran como es un gran error intentar extrapolar el comportamiento de un compuesto es un medio de reacción a otro medio totalmente diferente. Además de conocer la estructura de una molécula a diferentes pHs, concentraciones, etc. es imprescindible conocer las interacciones nutriente-nutriente, fármaco-nutriente, etc.
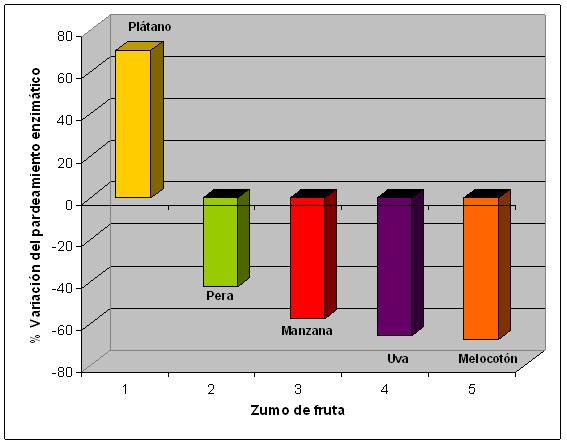
Porcentaje de variación del pardeamiento enzimático de distintos zumos de frutas en presencia de maltosyl-β-CD 90 mM.
Pero la conclusión más importante es la tercera. Las ciclodextrinas, mis moléculas preferidas, aquellas con las que mantengo una relación sentimental desde hace casi 20 años, tienen doble cara y no te puedes fiar de ellas ya que según con quien se codeen se portan de una forma u otra. Son «más falsas que Judas»…molan.
Jose
Nota: Esta es mi segunda entrada en la XI Edición del Carnaval de la Química que durante este mes de Enero de 2012 se alberga en el blog La Aventura de la Ciencia. Además participa en la IX Edición del Carnaval de la Biología que se aloja este mes en el blog La Ciencia de la Vida y en la VI Edición del Carnaval de la Tecnología que organiza un servidor en Scientia.
Fuentes:
- López-Nicolás et al. Kinetic Study of the Activation of Banana Juice Enzymatic Browning by the Addition of Maltosyl-B-cyclodextrin. J. Agric. Food Chem. 2007, 55, 9655–9662.
- López-Nicolás et al. Use of Natural and Modified Cyclodextrins as Inhibiting Agents of Peach Juice Enzymatic Browning. J. Agric. Food Chem. 2007, 55, 5312-5319.
- López-Nicolás et al. Use of Cyclodextrins as Secondary Antioxidants to Improve the Color of Fresh Pear Juice. J. Agric. Food Chem. 2007, 55, 6330-6338.
- López-Nicolás et al. Kinetic model of apple juice enzymatic browning in the presence of cyclodextrins: The use of maltosyl-β-cyclodextrin as secondary antioxidant. Food Chem. 101, 2007, Pages 1164–1171.







Muy interesante aunque viendo las fuentes no me fiaría mucho! 😉
Gracias Fabrizio. Estoy de acuerdo contigo, el que encabeza esos comentarios es mala gente… 😉
Un artículo excelente, Jose. Divulgación de primera. Necesita un mínimo nivel, pero si lo tienes es de lo más estimulante… y curioso.
Enhorabuena. Y gracias.
PD.- Algún día tendrás que sacar del armario a todos los «et al» de tus publicaciones 😛
¿Te ha gustado? Como dije en el decálogo de la divulgación creo que es necesario que contemos a la sociedad a qué nos dedicamos y para qué sirven nuestras investigaciones.
ah!! Los «et. al» veces no quieren salir en estas cosas…»cosas veredes».
Un abrazo compañero!!
Desde la ignorancia del profano en estas artes…
Si los polifenoles libres en el medio son oxidados enzimaticamente, su concentración en el medio disminuye y por lo tanto el equilibrio de la reacción de encapsulación se desplaza hacia la liberación de la especie retenida. ¿No estamos entonces ante otra solución temporal como la adición de ácido ascórbico?
Hola! está claro que muy profano no eres porque la pregunta así lo indica. Te contesto. Los experimentos realizados muestran como la capacidad de ralentización del pardeamiento enzimático empleando las ciclodextrinas es mucho mayor que la del ácido ascórbico. Sin embargo, hemos demostrado en el laboratorio que la mejor solución es el uso conjunto del ascórbico y cicldextrinas ya que éstas actúan como antioxidante primario fente a los polifenoles y secundario frente al ascórbico…y todo esto para productos de cuarta gama principalmente que no llevan tratamiento térmico que inhiba a la enzima.
Un saludo y gracias por tu aportación.
Creo que estoy teniendo un «Déjà vu».
Firmado:
Una alumna de Bioquímica
Pues no me he enterado…
Firmado:
Un profesor de Bioquímica
yo como estudiante de biotecnología sí he tenido un «Déjà vu». Me viene a la mente preparar zumo de pera en un laboratorio, medir absorbancias y hacer una valoración organoleptica del zumo con distintas concentraciones de antioxidantes.
Buen post, algo realmente sorprendente. Hasta en las frutas encuentra uno sorpresas científicas inesperadas.
¿Inesperadas? Las frutas te darían muchas sorpresas científicas…buenas y malas
Un saludo Adrián
Muy buen post, he disfrutado como hacía tiempo que no lo hacía con esta mezcla de divulgación, lectura amena y rigor científico. Para ser sincero, ni siquiera conocía las ciclodextrinas… perdóneme usté. Pero al pinchar en el link ya veo que todas las posibilidades que se me iban ocurriendo las has ido desgranando, así que nada xD
Ya para terminar… me he dado cuenta de que no se casi nada sobre oxidantes. Me he pasado 5 años estudiando el editado postranscripcional del mRNA, el proyecto genoma y las experiencias del principio transformante de Griffith (estas tres cosas, invariablemente, se han repetido durante los 5 años de carrera), pero nadie me ha contado casi nada sobre oxidantes… En fin…
Obviamente, cuando digo oxidantes me refiero a antioxidantes y tal. Mis conocimientos en química son rudimentarios, pero a las reacciones redox típicas que aparecen por todos los lados en bioquímica llego xD
Eran las 9 de la noche, ya no estoy para estos trotes…
Te había entendido perfectamente. Un saludo y me alegro que te haya gustado. Gracias por seguir el Blog.
Pingback: El antioxidante que se pasó al lado oscuro con la ayuda de un plátano
Aquí otro fan de las ciclodextrinas… aunque ya sabía que no es oro todo lo que reluce jjejeje
Un artículo muy interesante y divulgativo!
Me gustaría saber si tienes datos acerca de la variación organléptica de los zumos al añadir las BCD y si has realizado alguna estimación del coste de proceso… quiero decir del incremento de precio del producto final con la adición de BCD…
GRAN POST!
Claro que hay datos…. y dentro de poco los pondré en un post aunque ya están publicados en artículos científicos.
Un saludo!
Muy buen post… de lo que se entera uno… pero me han surgido varias preguntas…
Por lo que he leído el oscurecimiento del plátano, mayormente, es debido a la oxidación de la dopamina… pero por lo que he dado en fisiología molecular de plantas, el etileno es una de las fitohormonas responsables de la maduración y por lo tanto… del oscurecimiento. ¿Tiene algo que ver esta fitohormona con la inhibición de los inhibidores de la polifenoloxidasa? ¿O actua como prooxidante de la dopamina y demás compuestos fenolicos?
Muchas gracias y sigue así 😉
El etileno se ha demostrado que activa la polifenoloxidasa de plátano.
Aquí tienes un ejemplo. Gracias por tu enriquecedor comentario:
http://sciencelinks.jp/j-east/article/200115/000020011501A0457788.php
Magnífico artículo Jose, he disfrutado como un enano leyéndolo! No sabía que los plátanos tenían dopamina. Espero que la industria alimentaria no te tome la palabra ahora y pida un claim a la EFSA para prevención del Parkinson…
Otra cosa que tampoco sabía era que la mayoría de los polifenoles son hidrofóbicos, pensaba que era al contrario.
Gracias por la clase y espero la siguiente.
Un saludo!
Gracias!!
No se puede generalizar.Además, muchos polifenoles tienen una parte hidrofóbica (la que entra en la cavidad interna de las ciclodextrinas) y otra hidrofílica.SIn embargo tenemos la costumbre de ver grupos hidroxilo en una molécula y pensar que es muy hidrofílica.Un ejemplo es el resveratrol con 3 grupos -Oh y altamente hidrofóbico.
Un saludo y gracias por tus comentarios!!
Pingback: Resumen del VI Carnaval de la Tecnología | SCIENTIA
Enhorabuena Jose!
Me encanta tu página y aprendo muchísimo. Una sugerencia, me encantaría tener las entradas en formato pdf para poder imprimirlas, guardarlas y poderlas releer tranquilamente sentada en el sofá… Una que es muy clásica y le encanta el papel y poder subrayar y hacer anotaciones y garabatos.
Un abrazo:
ISA
Me ha encantado el artículo, de hecho me diste la idea de los zumos para investigar un poquito más para mi defensa de máster (que salió estupendamente). Gracias por seguir instruyéndome sobre este mundo, te seguiré leyendo con interés. Un saludo.
Me encanta como escribes y como describes de manera sencilla el uso de las ciclodextrinas en los zumos. La verdad es que tus lecturas enganchan un monton!!!
Qué sorpresa!!Muchas gracias y a ver como te animas que si alguien que escribe de maravilla eres tu!!
Un abrazo!!
disculpe… como sigo su blog mmm no se mucho de esto pero si me interesa saber un poco mas del pardeamiento enzimatico
Pingback: Gimli, el enano bioencapsulado por culpa de su mal olor | SCIENTIA
Pingback: Gimli, el enano bioencapsulado por culpa de su mal olor | SapienScientia
La dopamina se encuentra en iguales concentraciones en la Cascara que en la pulpa de la fruta digamos..?? 🙂