A estas alturas del año, seguro que todos ustedes saben, y si no es así no merecen ser lectores de este blog, que la Real Academia de Ciencias de Suecia ha otorgado el Nobel de Química 2013 al investigador austríaco Martin Karplus, al sudafricano Michael Levitt y al israelí Arieh Warshel por el “desarrollo de modelos multiescala de sistemas químicos complejos”…. cosa que es muy posible que a alguno de ustedes les suene a chino.
La concesión a estos tres investigadores de la máxima distinción científica en el campo de la alquimia ha levantado mucha polémica, pero desde mi punto de vista es más que merecida ya que sus descubrimientos en el campo de la química computacional están siendo de vital importancia en el desarrollo de muchas otras áreas científicas, lo que está repercutiendo positivamente en el día a día de los ciudadanos… y hoy se lo voy a demostrar con un ejemplo. ¿Cómo puede influir la química computacional en que tengamos menos riesgo de morir por una trombosis? Vayamos por partes.
 La trombosis es un proceso patológico por el que un agregado de plaquetas o fibrina ocluye un vaso sanguíneo y que puede tener consecuencias fatales. Como bien es sabido, uno de los tratamientos más empleados para prevenir los coágulos de sangre, y por tanto reducir los riesgos de ataque al corazón, accidente cerebrovascular y embolia pulmonar, es el uso de heparina, un anticoagulante usado en varios campos de la medicina y que actúa como cofactor de la antitrombinaIII. Al unirse la heparina a la antitrombinaIII se produce una activación de esta última, lo que provoca la inhibición natural de la trombina, enzima perteneciente al grupo de las peptidasas y responsable de la formación de trombos.
La trombosis es un proceso patológico por el que un agregado de plaquetas o fibrina ocluye un vaso sanguíneo y que puede tener consecuencias fatales. Como bien es sabido, uno de los tratamientos más empleados para prevenir los coágulos de sangre, y por tanto reducir los riesgos de ataque al corazón, accidente cerebrovascular y embolia pulmonar, es el uso de heparina, un anticoagulante usado en varios campos de la medicina y que actúa como cofactor de la antitrombinaIII. Al unirse la heparina a la antitrombinaIII se produce una activación de esta última, lo que provoca la inhibición natural de la trombina, enzima perteneciente al grupo de las peptidasas y responsable de la formación de trombos.
A pesar de que su mecanismo de actuación está bastante establecido y la heparina es ampliamente usada, en los últimos años se ha incrementado la búsqueda de nuevos fármacos que posean mayor capacidad antitrombótica que la heparina y que no tengan efectos secundarios como algunos que se han descrito para este tradicional anticoagulante.
Hasta ahora la estrategia seguida para el desarrollo de novedosos medicamentos ha sido la síntesis química de nuevos compuestos o la modificación de los ya existentes. Sin embargo, estas estrategias son muy costosas y la efectividad no siempre está asegurada por lo que hay que buscar otras alternativas para el desarrollo de nuevos fármacos… y es aquí donde los señores Martin Karplus, Michael Levitt y Arieh Warshel vuelven a entrar en escena.
 En la década de 1970 los investigadores galardonados con el Premio Nobel de Química 2013 sentaron las bases de las metodologías teóricas que luego tradujeron a los potentes programas informáticos que son usados actualmente para comprender y predecir procesos químicos, unos modelos que replican la vida real y que se han convertido en uno de los avances más cruciales para la química contemporánea.
En la década de 1970 los investigadores galardonados con el Premio Nobel de Química 2013 sentaron las bases de las metodologías teóricas que luego tradujeron a los potentes programas informáticos que son usados actualmente para comprender y predecir procesos químicos, unos modelos que replican la vida real y que se han convertido en uno de los avances más cruciales para la química contemporánea.
Gracias a la química computacional desarrollada por nuestros tres protagonistas de hoy se pueden simular en ordenadores reacciones químicas complejas para predecir como pueden interaccionar determinadas moléculas o para saber si una reacción va a ocurrir o no, y este poder predictivo se emplea para muchas finalidades… entre las que se encuentra, tal y como acaban de demostrar en un artículo publicado en la revista Journal of Medicinal Chemistry (JMC) un grupo de investigadores españoles y alemanes, el diseño de nuevos fármacos que pueden combatir la trombosis con mayor efectividad que los medicamentos tradicionales.
¿Y cómo han empleado la química computacional este grupo de investigadores para el desarrollo de nuevos fármacos antitrombóticos?
Como he comentado anteriormente son varias las proteínas (trombinas y antitrombinas) que están relacionadas con el desarrollo, prevención o cura de los infartos de miocardio, accidentes cerebrovasculares y embolias pulmonares. Pues bien, los responsables del artículo publicado en JMC decidieron diseñar nuevos fármacos con actividad frente a antitrombina superior a la que posee la heparina, lo que aumentaría la efectividad contra la formación de trombos.
Para conseguir dicho objetivo su estrategia fue buscar una nueva molécula (ligando) que, al acoplarse a los receptores proteicos de la antitrombina, actuara como un interruptor molecular y regulara su actividad… pero esa tarea no fue nada fácil.
¿Cómo se puede encontrar el ligando ideal que se una a la antitrombina y disminuya la formación de trombos? ¿Es la única opción ir probando experimentalmente en el laboratorio con todos aquellos ligandos que creamos que pueden modificar positivamente la actividad de la antitrombina hasta dar con el más adecuado? ¿Qué tiempo me llevaría ese proceso? ¿Es rentable económicamente? ¿Hay otras formas de encontrar la aguja en el pajar?
La química computacional premiada con el Premio Nobel de Química 2013, a través del llamado cribado virtual, nos dará la respuesta a todas estas preguntas…
 El cribado virtual es el uso de herramientas de modelado molecular o química computacional para cribar in-silico (por computadora o vía simulación computacional) una librería que contiene información estructural sobre gran cantidad de ligandos (incluso decenas de millones de ellos). Un correcto cribado nos permitirá encontrar entre todos los componentes de dicha librería, y sin necesidad de ir probando uno por uno en el laboratorio, cuáles son los ligandos óptimos para unirse a la antitrombina capaces de modificar su actividad en mayor grado que lo que lo hace la heparina.
El cribado virtual es el uso de herramientas de modelado molecular o química computacional para cribar in-silico (por computadora o vía simulación computacional) una librería que contiene información estructural sobre gran cantidad de ligandos (incluso decenas de millones de ellos). Un correcto cribado nos permitirá encontrar entre todos los componentes de dicha librería, y sin necesidad de ir probando uno por uno en el laboratorio, cuáles son los ligandos óptimos para unirse a la antitrombina capaces de modificar su actividad en mayor grado que lo que lo hace la heparina.
Si ustedes están siguiendo correctamente el guión de este post estarán de acuerdo conmigo que para dar el primer paso que nos permita identificar aquellos candidatos a unirse con gran afinidad a una proteína diana, en nuestro caso antitrombina, “solo” necesitaremos una amplia librería donde buscar ligandos (que pueden llegar a estar compuestas por millones de compuestos químicos) y un potente ordenador que haga las simulaciones correspondientes.
 Como librería, el grupo de investigadores responsables del artículo publicado en JMC emplearon la “Zinc database and ligand library” donde pudieron cribar computacionalmente entre más de 13 millones de compuestos para seleccionar la molécula óptima para interaccionar con la antitrombina… ¿se imaginan probar en el laboratorio 13 millones de compuestos experimentalmente?
Como librería, el grupo de investigadores responsables del artículo publicado en JMC emplearon la “Zinc database and ligand library” donde pudieron cribar computacionalmente entre más de 13 millones de compuestos para seleccionar la molécula óptima para interaccionar con la antitrombina… ¿se imaginan probar en el laboratorio 13 millones de compuestos experimentalmente?
Vale, ya tenemos una extensa librería de posibles ligandos de la trombina… ¿y ahora qué?
Para poder procesar grandes librerías con millones compuestos, los métodos de cribado virtual deben ser lo suficientemente rápidos para poder realizar el proceso en un espacio de tiempo razonable y poder además identificar “las agujas en el pajar”. .. ¿y de qué métodos de cribado se dispone?
 Para realizar cribado virtual podemos usar muchas técnicas distintas, desde las más rápidas e imprecisas, tales como farmacóforos, como las de mediana precisión (docking), como las de precisión alta (dinámica molecular) y por último las de muy alta precisión (métodos cuánticos)… otras veces se suele hacer el cribado virtual en cascada: a) se parte de millones de compuestos que se procesan por docking, se seleccionan 1000; b) se realiza dinámica molecular con esos 1000 y se seleccionan 10; c) se realizan cálculos mecánico cuánticos con los 10 restantes.
Para realizar cribado virtual podemos usar muchas técnicas distintas, desde las más rápidas e imprecisas, tales como farmacóforos, como las de mediana precisión (docking), como las de precisión alta (dinámica molecular) y por último las de muy alta precisión (métodos cuánticos)… otras veces se suele hacer el cribado virtual en cascada: a) se parte de millones de compuestos que se procesan por docking, se seleccionan 1000; b) se realiza dinámica molecular con esos 1000 y se seleccionan 10; c) se realizan cálculos mecánico cuánticos con los 10 restantes.
De entre todos estos métodos el grupo de investigadores españoles y alemanes emplearon la técnica de docking molecular para realizar el cribado. En el campo del modelado molecular, este es un método que predice la conformación preferida de un molécula, al estar unida a otra, con el fin de formar un complejo estable.
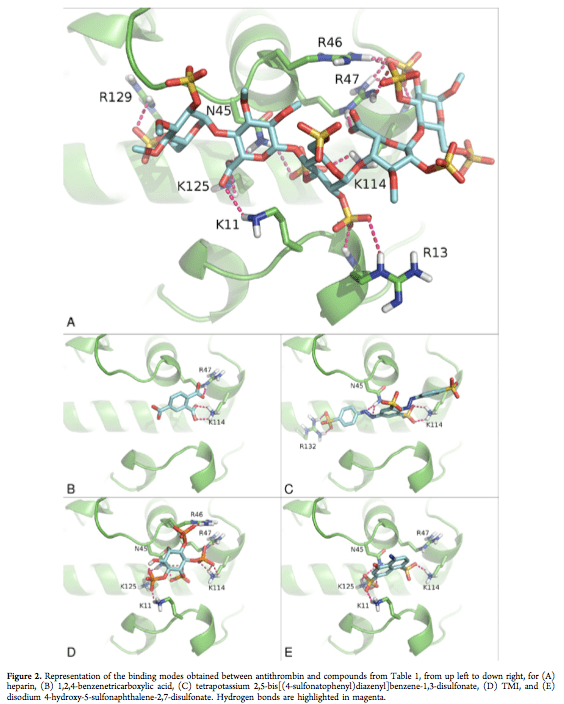
El conocimiento de la orientación preferida se empleó también para predecir la fuerza de la asociación usando las funciones de puntuación (o funciones de scoring). En la siguiente imagen pueden ver los cinco compuestos de la base de datos ZINC que obtuvieron mayor puntuación para unirse a la antitrombina.
De entre los más de 13 millones de candidatos para activar la antitrombina la molécula seleccionada para acoplarse con gran fuerza a la antitrombina con una puntuación casi el doble que la heparina fue el D-myo-iositol 3,4,5,6-tetrakisphosphate (TMI), una molécula que además no presenta los efectos secundarios que puede tener la heparina sobre la salud. En teoría, los investigadores ya disponían del compuesto ideal para sustituir a la heparina como nuevo fármaco antitrombótico… pero aun no había acabado el proceso.
Para que los resultados obtenidos mediante química computacional a través de grandes ordenadores sean definitivos deben complementarse con experimentos en los laboratorios que confirmen los resultados predichos. En el caso que nos ocupa los datos experimentales obtenidos mediante diferentes técnicas analíticas revelaron que el compuesto TMI tiene una afinidad por la antitrombina 6 veces mayor que la heparina tal y como se puede demuestra comparando los valores de afinidad (Kd) que se aprecian en la siguiente imagen.
Todo cuadraba. Bueno, todo no. Aun quedaban las pruebas de funcionalidad que demostraran que en la práctica el nuevo fármaco funcionaba mejor que al heparina… porque una cosa es que el TMI se una más fuerte a la antitrombina y otra muy distinta es que eso luego se traduzca en una mayor capacidad anticoagulante…. y los resultados no fueron los esperados.
A pesar de que el TMI interaccionaba fuertemente con la antitrombina no era capaz de activarla completamente y su capacidad anticoagulante era menor que la esperada. De hecho su capacidad de inhibición de la trombina era solamente un poco superior a la de la heparina… muy lejos de lo predicho. ¿Estaba todo perdido? No.
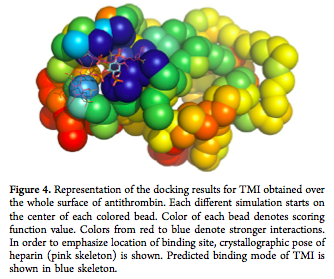 Los científicos siguieron investigando y se llevaron una gran sorpresa. Un experimento en el que se estudió la acción conjunta de la heparina y del TMI reveló un espectacular efecto sinérgico de ambas moléculas. Al unir el compuesto obtenido tras el cribado virtual, el TMI, a la antitrombina, se producía un cambio conformacional de esta última que favorecía la unión posterior de la heparina.
Los científicos siguieron investigando y se llevaron una gran sorpresa. Un experimento en el que se estudió la acción conjunta de la heparina y del TMI reveló un espectacular efecto sinérgico de ambas moléculas. Al unir el compuesto obtenido tras el cribado virtual, el TMI, a la antitrombina, se producía un cambio conformacional de esta última que favorecía la unión posterior de la heparina.
El resultado final era un gran incremento en la capacidad anticoagulante de la antitrombina fruto de la acción conjunta del TMI y de la heparina… lo que abre de par en par las puertas al desarrollo y comercialización de un nuevo fármaco anticoagulante tras los pertinentes estudios in-vitro, en animales y finalmente en ensayos clínicos en humanos. Gran trabajo.
Estimados lectores, personalmente son muchas las conclusiones que extraigo del post que ustedes acaban de leer.
 Por un lado el desarrollo de la química computacional está siendo de vital importancia para la predicción y desarrollo de infinidad de reacciones químicas de gran importancia por lo que la concesión del Premio Nobel a los padres de esta rama de la química está más que justificada.
Por un lado el desarrollo de la química computacional está siendo de vital importancia para la predicción y desarrollo de infinidad de reacciones químicas de gran importancia por lo que la concesión del Premio Nobel a los padres de esta rama de la química está más que justificada.
Por otra parte hemos de tener claro que la química computacional y la química experimental forman un binomio en el cual cada uno de los componentes se nutre del otro. La química computacional necesita a la experimental para corroborar sus predicciones y la química experimental necesita a la computacional para optimizar su rendimiento.
Pero la conclusión más importante que yo personalmente extraigo es la siguiente. En este post les he mostrado como en un solo trabajo un grupo de investigadores emplea herramientas pertenecientes a campos tan “teóricamente” distintos como la química, la informática, la medicina, la bioquímica, la farmacología, las matemáticas… lo que me ha servido para ratificarme en algo que llevo pensando muchos tiempo: en los tiempos que corren parcelar áreas científicas tiene cada vez manos sentido. El trabajo multidisciplinar es el futuro del avance científico. Sigamos por este camino.
Jose
*Este post participa en la XXVIII Edición del Carnaval de Química que organiza Flagellum .
Nota: Quiero agradecer muy especialmente la colaboración en la redacción de este post de Horacio Pérez Sánchez, miembro del equipo investigador responsable del trabajo citado en esta entrada (http://bio-hpc.eu).
Referencia: In Silico Discovery of a Compound with Nanomolar Affinity to Antithrombin Causing Partial Activation and Increased Heparin Affinity. J.Navarro-Fernańdez, H.Peŕez-Sańchez, I.Martínez-Martínez, I.Meliciani, J.A.Guerrero, V. Vicente, J. Corral, and W. Wenzel. Journal of Medicinal Chemistry. 2012, 55, 6403−6412.







Muy buena entrada.
Este es el futuro de la farmacología y de la medicina, sin lugar a dudas.
Gracias por redactarlo todo de manera tan clara y enhorabuena también por la labor de divulgación de alta calidad que realizas.
Gracias David 😉
Muy bueno si señor, yo he trabajado en química computacional y cuando lo contabas siempre te venía alguno a preguntar «¿y eso pa que sirve?». Excelente explicación.
Ya tienes una explicación que les puede convencer 😉
Enhorabuena, excelente artículo. Yo he trabajado en química computacional, y cuando lo explicabas siempre te preguntaba alguien «¿y eso pa que sirve?»
Fantástico post. Creo que es un mensaje que se debe potenciar, está más que claro que sin multidisciplinaridad no hay ciencia que valga. Los mejores trabajos aúnan la utilización de modelos informáticos con la comprobación experimental; personalmente es un orgullo que el trabajo de mi tesis precisamente ganase en robustez al combinar técnicas bioinformáticas y análisis filogenéticos con biología molecular básica para comprobar lo que los datos obtenidos con estas técnicas nos indicaban. Más adelante he usado este mismo abordaje en todos los trabajos que he podido, como comentaré más pronto que tarde en el blog.
Y en el campo de la química y el análisis de estructuras moleculares es TAN evidente… las aplicaciones prácticamente surgen solas, cuando tienes a tu disposición esta combinación de herramientas.
Me parece un Nobel más que acertado, estoy un poco harto que entre los mismos científicos a veces s emenosprecien datos por estar obtenidos con técnicas distintas: «ah, sí, pero ese trabajo se hizo sólo in vitro… oh vaya, pero es un mero análisis informático»; bueno, la cosa es que hay que combinar técnicas, ninguna en sí misma es la panacea pero cada una aporta una visión complementaria e indispensable para entender el todo.
Hablamos el mismo idioma…como siempre. Gracias por comentar Carlos 😉
Jose, me alegro mucho de que hayas escrito un post como éste, sinceramente. Y te diré por qué. Verás, mi área de trabajo actual está muy relacionada con la química computacional, aunque no te lo creas. Sabes que me dedico a simular materiales para reactores nucleares de fisión, es decir, hago física computacional. Pero lo que no sé si sabes también es que lo que en mi grupo nos dedicamos a estudiar, entre otras cosas, son las reacciones que pueden sufrir el hidrógeno o el helio (sí, esos elementos de números atómicos 1 y 2 en la Tabla Periódica, respectivamente), si forman burbujas, si forman aglomerados que puedan dañar la estructura de las paredes del reactor, etc.
Después, nuestros cálculos «ab initio» les sirven a otras personas que llevan a cabo la dinámica molecular de la que hablas en tu post, o también simulaciones de Monte Carlo. Es decir, entre todos hacemos modelado multiescala.
Como te digo, me ha encantado tu artículo porque acerca un poco a la gente todo este mundo tan desconocido y muchas veces incomprendido de la simulación mediante ordenador, algo que es fácilmente entendible con lo que tú has dicho, es decir, resulta completamente imposible «testar» miles de compuestos, reacciones, efectos y demás situaciones de forma práctica, tanto en el laboratorio como en un reactor nuclear, como es mi caso. ¿Quién, en su sano juicio, probaría a bombardear con neutrones las paredes de un reactor, bajo riesgo de agrietarlas y producir una catástrofe, por ponerme en un caso enormemente improbable, pero que sirve perfectamente para entender el asunto? No hay ni dinero que sufrague esas pruebas ni científicos tan locos como para llevarlas a la práctica. Y es por ello que la ciencia computacional (en la rama que sea) se ha hecho imprescindible e insustituible en este mundo tan maravillosamente interdisciplinar.
Abrazo.
No sabía esto que me has contado Sergio. Me alegro muchísimo que escribas de tus propias investigaciones… y más aun de compartir fundamentos y formas de ver el progreso científico.
Un abrazo
Y yo pregunto:
¿La asociación de la heparina con el TMI está libre de efectos secundarios? ¿Por qué no se podría valorar tambien el uso de TMI individualmente en lugar de tratamientos de heparina en casos en los que la acción anticoagulante requerida no sea «extrema» y así evitar los efectos secundarios derivados de la heparina?
Genial post, genial explicación. Excelente trabajo!
Es el momento de experimentar lo que preguntas. Estaremos atentos. Gracias 😉
Las posibilidades de todo esto son acojonantes… Ya me imagino el día en que vayamos al médico de cabecera, y a partir de una muestra de sangre o saliva meta nuestro ADN en un ordenador que analizará automáticamente qué fármaco se nos adapta mejor, lo sintetizará y nos dará la pastillita personalizada.
ehhhh…poco a poco. 😉
Genial entrada, y excelente trabajo. Felicidades!!
Gracias a ti por comentar.
Me ha gustado mucho la entrada, especialmente porque yo me dedico al área de la química computacional y cada vez voy cobrando más certeza de su importancia. Solo un pequeño apunte: desgraciadamente no siempre se puede reproducir en el laboratorio lo establecido a nivel computacional. En mi caso trabajo con la reactividad de radicales libres con los distintos puntos reactivos de una molécula y esto no tiene reproducción experimental; en el laboratorio solo podemos determinar la capacidad antioxidante global de la molécula pero no por posiciones o átomos puntuales. Un saludo.
Oye pues tenemos que hablar porque yo determino también la capacidad antioxidante de diferentes moléculas mediante varios métodos…colaboremos!!
Interesante trabajo
Lo es…
Reblogueó esto en La Química en el siglo XXIy comentado:
¿Cómo puede influir la química computacional en que tengamos menos riesgo de morir por una trombosis?
Pingback: Premio Nobel de Química 2013 | Actualidad informática
Me alegra que este Post reuna un pensamiento en común sobre la estructura, explicación e importancia de la Química teórica y Computacional. Actualmente trabajo en Química teórica y computacional de complejos inorgánicos y cada día se transforma en una pasión. En muchos congresos, encuentros y demás que he asistido a cobrado un protagonismo resaltado en todas las áreas y el premio nobel abre la puerta a aquellos científicos que todavía le temen a esta hermosa rama de Ciencia. Saludos desde Colombia. 😉
Pingback: El origen de los Uruk-Hai o el día que Sauron exterminó a sus Orcos con jasmonato para producir resveratrol | SCIENTIA
Muy interesante y clarito el post, como de costumbre.
Sólo quería compartir mi poca capacidad divulgativa en un detallito: me imagino que cuando hablas de «librerías» te refieres a «bibliotecas». Yo también caigo millones de veces en ese «false friend», y eso que llevo veinte años peléandome con el inglés y la informática. Pero bueno, pasito a pasito hacemos el camino.
Pingback: ¿Poder curar el cáncer desde la pantalla de tu ordenador? | Triplenlace
Pingback: La noche en la que Sauron sedujo a Arwen usando flores anti-inflamatorias | SCIENTIA