En el post de hoy Xabi Gutiérrez, Yanko Iruín (con el que he escrito este post a medias) y un servidor, les vamos a enseñar el fundamento científico que se esconde detrás de un proceso muy artesanal de elaboración de helados. Además, si ustedes leen la entrada hasta el final, van a aprender un “truco científico” que les servirá para ganar más de una apuesta. Atentos que llega la física.
Actualmente es muy fácil elaborar helados gracias a los potentes congeladores de los que disponemos pero antiguamente los heladeros no tenían a su alcance la tecnología moderna, por lo que estaban obligados a ingeniárselas de otra forma. Un ejemplo muy curioso es el que ustedes pueden ver en este video donde Xabi emplea una heladora de mitad del siglo XX que nos ha cedido el Ayuntamiento del bonito municipio vizcaíno de Orozco. En ella, y gracias a la “ciencia de los puntos eutécticos” de la que les hablaré a continuación, mi compi ha elaborado un sabrosísimo helado de vainilla y soja. Pasen y vean el nuevo vídeo de la sección «Ciencia en la cocina» del programa de TVE 2 «Órbita Laika».
La heladora tradicional que ha empleado Xabi está compuesta por una cuba de madera, una manivela y un calderín de metal. Tiene un mecanismo simple y muy similar al de los recipientes que vemos en los bares para batir horchata o limón granizado. Como se puede ver en el video la heladora dispone de una cuba de madera que rodea al calderín metálico. Los principales ingredientes del helado (leche, nata, azúcar, huevo, salsa de soja y vainilla) son vertidos dentro del recipiente de metal y se van mezclando gracias a varias hélices movidas con la manivela. Por otra parte, en el espacio que queda entre el cilindro de madera y el metálico se añade hielo… y sal.
La base científica del proceso de elaboración del helado tiene el bonito nombre de “mezcla eutéctica”. ¿De qué les estoy hablando? Tal y como nos cuenta Yanko Iruín en esta entrada publicada en su bitácora El Búho del Blog, en términos de la Química Física se conoce como mezcla eutéctica “a la que se da entre dos sustancias que, a una cierta proporción entre ellas, congela a una temperatura inferior a la que congelan las sustancias que la componen”.
Cuando Xabi coloca únicamente hielo en el espacio que queda entre el cilindro de madera y el de metal, y parte de ese hielo funde,… ¿a qué temperatura se alcanza el equilibrio entre el hielo y el agua líquida? La respuesta es sencilla: a 0º centígrados ya que tenemos un equilibrio entre dos fases de un componente puro. Este equilibrio se mantiene mientras haya agua líquida y hielo.
Ahora bien, si queremos bajar la temperatura de la heladora artesanal por debajo de 0º C… ¿cómo podemos hacerlo? Añadiendo sal al espacio existente entre el cilindro de metal y el de madera donde se encuentra el hielo en equilibrio con el agua líquida. ¿Y eso por qué? Porque ahora tenemos un nuevo equilibrio. En él participan el hielo por un lado y una disolución de agua y sal (salmuera) por otro.
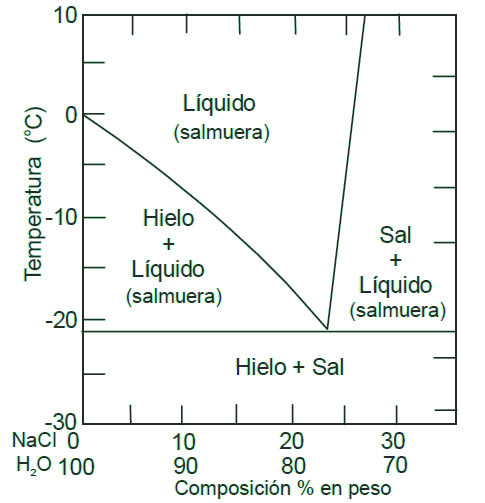
La temperatura de equilibrio del sistema hielo/agua+sal dependerá de la cantidad de sal disuelta en el agua. De hecho puede alcanzarse una temperatura de -21º cuando la salmuera tiene un 23% de sal. En ese momento aunque se añada más sal a la heladora ya no baja más la temperatura. Es lo que se conoce como punto eutéctico. Es un punto singular, en el que empieza a aparecer una tercera fase, la sal sólida. Por debajo de la temperatura del punto eutéctico (que se puede alcanzar enfriando la mezcla con algún dispositivo), solo existen hielo y sal, ambos sólidos y separados en fases bien diferenciadas.
En la siguiente imagen pueden observar el «diagrama de fases sólido/líquido del sistema binario constituido por sal y agua”.
De dicha imagen se pueden extraer, entre otras cosas, dos tipos de información muy relevantes:
- La temperatura del sistema hielo/salmuera dependiendo de la concentración de sal presente en la salmuera.
- El estado («líquido», «hielo + salmuera» o «sal + salmuera») del sistema hielo/salmuera dependiendo de la concentración de sal presente en la salmuera.
En un principio tenía pensado acabar el post de hoy aquí. Sin embargo, tras la emisión de este vídeo en el programa “Órbita Laika” muchas personas me preguntaron en las redes sociales acerca del uso de la sal para “fundir” el hielo presente en las carreteras tras una nevada.
Según ellos, si en el video se puede observar como la adición de sal sirve para disminuir la temperatura…¿cómo es posible que para deshacer el hielo se añada sal a las carreteras? ¿no bajaría aun más la temperatura y el hielo seguiría presente?
La respuesta a estas preguntas nos las vuelve a dar el «diagrama de fases sólido/líquido del sistema binario constituido por sal y agua”. Observen la siguiente imagen. Me la ha cedido el asesor científico del programa, mi amigo y maestro Yanko Iruín. Corresponde a una de las diapositivas que les muestra a sus alumnos de la Facultad de Química de la UPV/EHU.
En ella se puede observar como no existe contradicción entre lo explicado en el vídeo de ¨Órbita Laika» para elaborar helados caseros y el sistema que se emplea para “fundir” el hielo de las carreteras. Veamos.
Fíjense en la línea roja que ha dibujado Yanko en su diapositiva y que está situada a una temperatura alrededor de unos diez grados bajo cero o 263 K, temperatura a la que se puede formar hielo las carreteras. Cuando la concentración de sal presente en el sistema es baja estamos en la zona descrita como “Hielo + Disolución”, en la que parte del hielo de la carretera se fundirá al verter sal, formando una disolución que estará en equilibrio con hielo. Es una situación similar a la descrita en la elaboración casera de helados. Pero si la cantidad de sal es más grande, acabaremos saliéndonos de esa región “Hielo+Disolución” y entrando en otra en la que sólo pone “Disolución”, lo que quiere decir que TODO el hielo presente en la carretera se acabará fundiendo para acabar formando, únicamente, una disolución de sal en agua.
Por esta razón es tan importante que la cantidad de sal que los servicios municipales vierten en caso de heladas sea la adecuada para entrar en la zona “Disolución”. Si no, verter sal solo sirve para corroer los bajos del automóvil.
¿Qué les parece? ¿A que no sabían que dependiendo de la cantidad de sal empleada podemos provocar dos fenómenos aparentemente contradictorios como bajar la temperatura de una disolución o eliminar el hielo de una carretera? ¿Molan estos químico-físicos, eh? No sólo de bioquímica vive el hombre…aunque casi.
Lo prometido es deuda. Les he dicho anteriormente que si aguantaban hasta el final del post Xabi, Yanko y yo les íbamos a hacer ganar dinero. Hagan una apuesta con sus amigos para ver quien es capaz de enfriar más rápido una botella de champagne.
 Lo normal es que ellos intenten hacerlo en un congelador de gran potencia. Ustedes metan la botella en un simple cubo que lleve agua, hielo y alcohol. ¿Quienes ganarán la apuesta? Ustedes. Tanto con los congeladores como con el sistema “hielo/disolución de alcohol en agua” se pueden alcanzar temperaturas similares (alrededor de los -23ºC). Sin embargo, la velocidad de enfriamiento es mayor en la opción que han elegido ustedes que en la de sus amigos. ¿Por qué? Porque la disolución de alcohol en agua en contacto con la botella es mas eficiente a la hora de conducir el calor que el aire con el que está en contacto la botella en un congelador. Por este motivo ustedes llegarán antes a los -23ºC que sus amigos. Fácil.
Lo normal es que ellos intenten hacerlo en un congelador de gran potencia. Ustedes metan la botella en un simple cubo que lleve agua, hielo y alcohol. ¿Quienes ganarán la apuesta? Ustedes. Tanto con los congeladores como con el sistema “hielo/disolución de alcohol en agua” se pueden alcanzar temperaturas similares (alrededor de los -23ºC). Sin embargo, la velocidad de enfriamiento es mayor en la opción que han elegido ustedes que en la de sus amigos. ¿Por qué? Porque la disolución de alcohol en agua en contacto con la botella es mas eficiente a la hora de conducir el calor que el aire con el que está en contacto la botella en un congelador. Por este motivo ustedes llegarán antes a los -23ºC que sus amigos. Fácil.
Eso sí, cuando ganen la apuesta recuerden que lo han hecho gracias a las mezclas eutécticas… y a este post publicado por Yanko Iruín en el “El Búho del blog” donde aprendí lo que les he contado.
Jose
Nota: Una vez más me gustaría recordar que los videos de “Ciencia en la cocina” han sido realizados por K2000 para la Cátedra de Cultura Científica de la UPV/EHU. En los siguientes enlaces pueden ver los anteriores capítulos de esta serie.
2.- Frutas pomposas bajo un volcán de caseínas
3.- El carbón dulce de los Reyes Magos
4.- Postre fractal con hidromiel
5.- Ensalada de chile camuflado con carragenano y ácido carmínico







Y agua con sal para la apuesta? Yo lo había hecho cuando trabajaba de camarero y se nos había olvidado recargar la cámara con vino la noche anterior.
Con agua y sal tendrías un problema gordo. Para llegar a -20ºC (ejemplo) necesitarías un porcentaje de sal demasiado grande y aparecerían problemas de cristalización. EL congelador sin embargo llega fácilmente Por eso mejor emplear alcohol ya que el punto estético de hielo/algua-alcohol es muy bajo y no existen esos problemas descritos anteriormente.
¿Qué tipo de alcohol y en que proporción?
¿Vale el alcohol de 70°?
Pingback: Ciencia en la Cocina (VII): La aparente contrad...
Unos ejemplos estupendos para cuando nos toque explicar el fenómeno de la crioscopia y que l@s alumn@s lo entiendan con cosas prácticas. Gracias
muy bien el artículo , como siempre
mi pregunta es ¿ con que % de agua , hielo y alcohol se debe empezar la apuesta ? , para ganarla
saludos cordiales
Aqui tienes la respuesta: http://elblogdebuhogris.blogspot.com.es/2009/05/mas-sobre-mezclas-frigorificas.html
Un saludo!
Pingback: La aparente contradicción entre los helados eutécticos y el deshielo de carreteras
Gracias. Lo he tenido que releer varias veces pero lo he entendido. Una cosita: ¿como calculan la cantidad de sal que hay que hechar en la carretera? O la saturan directamente…
Tanto el capítulo de órbitalaika como este post, me trajeron muchísimos recuerdos , precisamente de los años cincuenta del siglo pasado…Hacíamos helados en una heladora como la que usaron ustedes, porque donde vivía no había luz…por lo tanto, no había hielo, pero acarreaban un témpano desde un ventisquero, se guardaba en un hoyo en el jardín, y había hielo para varios días…o si no, aprovechábamos la nieve del invierno…las estalactitas que colgaban de los techos…el ingenio se aprovechaba también…y la variedad iba desde los helados de vainilla, lo de chocolate, plátano o lo que fuera.
Gracias por estos recuerdos, y gracias por las explicaciones.
Emocionante…gracias a ti!
Pingback: Ciencia en la Cocina (VII): La aparente contradicción entre los helados eutécticos y el deshielo de carreteras
Pingback: Ciencia en la cocina: helado eutéctico de vainilla y soja | Ciencia en la cocina | Cuaderno de Cultura Científica
Pingback: Ciencia en la Cocina (VIII): Crómlech de mandioca al cianuro de hidrógeno | SCIENTIA
Pingback: Resumen Scientia [Febrero 2015] | SCIENTIA
Pingback: La “Ciencia en la Cocina” de Órbita Laika explicada en 12 vídeos | SCIENTIA
Pingback: 12 posts correspondientes a los 12 vídeos | ONG AFRICANDO SOLIDARIDAD CON AFRICA
Pingback: Ciencia en la Cocina (VII): La aparente contrad...