Terminamos la semana con un nuevo vídeo de “Ciencia en la cocina”, la sección científico-culinaria del programa de TVE 2 “Órbita Laika” . Como conocen los fieles seguidores de Scientia en mis apariciones en el programa suelo dar pinceladas sobre algunos conceptos científicos, referidos tanto a procesos como a ingredientes, que se esconden detrás de los platos que prepara Xabi Gutiérrez (responsable de innovación del Restaurante Arzak). En los posts que publico posteriormente, como es el caso de hoy, me extiendo más en la ciencia que hay en cada preparación culinaria.
En esta ocasión Xabi “juega” con un gas (el tetrafluoroetano) y dos de mis debilidades (el chocolate y el oro) para elaborar «trufas doradas al tetrafluoroetano». Pasen y vean.
El chocolate es el alimento que se obtiene mezclando azúcar con dos productos derivados de la manipulación de las semillas del cacao: la pasta de cacao y la manteca de cacao. Estructuralmente podemos decir que este exquisito manjar es un compuesto terciario de tres sólidos en disolución: los sólidos de cacao, el azúcar cristalizado y la manteca. Esta última es la grasa natural comestible procedente del haba del cacao extraída durante el proceso de fabricación del chocolate y que se separa de la masa de cacao mediante presión.
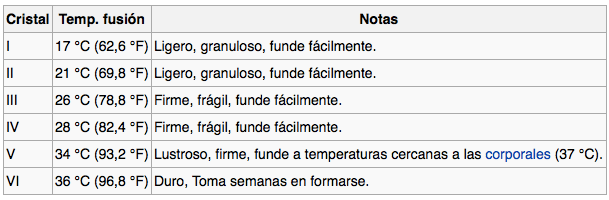
 Un dato importante es que la manteca posee seis estructuras cristalinas que se indican con las letras romanas del I al VI, que tienen puntos de fusión de 17°, 21°, 26°, 28ºC, 34º y 36° C respectivamente. La proporción de las estructuras cristalinas en la manteca, y por tanto en el chocolate, depende mucho del origen del cacao y de las condiciones en las que se ha enfriado el chocolate fundido. Pues bien, como dice Xabi en el vídeo, previamente a la elaboración de las trufas doradas al tetrafluoroetano se necesita aplicar una temperatura de aproximadamente 33ºC para fundir el chocolate sólido y generar el líquido.
Un dato importante es que la manteca posee seis estructuras cristalinas que se indican con las letras romanas del I al VI, que tienen puntos de fusión de 17°, 21°, 26°, 28ºC, 34º y 36° C respectivamente. La proporción de las estructuras cristalinas en la manteca, y por tanto en el chocolate, depende mucho del origen del cacao y de las condiciones en las que se ha enfriado el chocolate fundido. Pues bien, como dice Xabi en el vídeo, previamente a la elaboración de las trufas doradas al tetrafluoroetano se necesita aplicar una temperatura de aproximadamente 33ºC para fundir el chocolate sólido y generar el líquido.
Pasemos a hablar del tetrafluoroetano (1,1,1,2-tetrafluoroetano), un gas inerte que se encuentra dentro del aerosol que Xabi continuamente me quiere quitar de las manos, cuya fórmula es CH2FCF3, y que posee un punto de -26,3 C a presión atmosférica de ebullición. Voy a contarles algo de su historia.
 Los refrigerantes químicos usados para los refrigeradores antes de 1930, eran habitualmente propano, isobutano y ciclopentano. A partir de los años 30 los clorofluorocarbonos o CFC, compuestos que contienen átomos de cloro, aparecieron en escena. Durante mucho tiempo los CFC fueron ampliamente usados en la industria como refrigerantes (siendo los más conocidos el diclorodifluorometano y el clorodifluorometano), propelentes y disolventes de limpieza. Sin embargo, los CFC suelen tener un alto potencial para reducir el ozono gracias principalmente a la ruptura de los enlaces carbono-cloro. Por ello su incidencia en el medio ambiente es muy negativa y su uso está actualmente prohibido casi totalmente por el Protocolo de Montreal.
Los refrigerantes químicos usados para los refrigeradores antes de 1930, eran habitualmente propano, isobutano y ciclopentano. A partir de los años 30 los clorofluorocarbonos o CFC, compuestos que contienen átomos de cloro, aparecieron en escena. Durante mucho tiempo los CFC fueron ampliamente usados en la industria como refrigerantes (siendo los más conocidos el diclorodifluorometano y el clorodifluorometano), propelentes y disolventes de limpieza. Sin embargo, los CFC suelen tener un alto potencial para reducir el ozono gracias principalmente a la ruptura de los enlaces carbono-cloro. Por ello su incidencia en el medio ambiente es muy negativa y su uso está actualmente prohibido casi totalmente por el Protocolo de Montreal.
Debido a los problemas planteados por los CFC comenzaron a emplearse los hidrofluorocarburos (HFC), hidrocarbonos en los que algunos de los átomos de hidrógeno han sido reemplazados por átomos de flúor que no dañan la capa de ozono. Así, HFC como el tetrafluoroetano se han convertido en sustitutos favoritos de los CFC… aunque también es cierto que el Protocolo de Kioto atribuye a los HFC problemas asociados al calentamiento global.
 ¿Y qué usos tiene el tetrafluoroetano? Este gas (inodoro, incoloro, no corrosivo, no irritante y no inflamable) se usa habitualmente como refrigerante tanto en aparatos caseros como en el aire acondicionado de automóviles. También se ha empleado en las industrias del plástico, farmacéutica, de los productos de limpieza, etc.
¿Y qué usos tiene el tetrafluoroetano? Este gas (inodoro, incoloro, no corrosivo, no irritante y no inflamable) se usa habitualmente como refrigerante tanto en aparatos caseros como en el aire acondicionado de automóviles. También se ha empleado en las industrias del plástico, farmacéutica, de los productos de limpieza, etc.
Pues bien, en la elaboración de nuestro plato el tetrafluoroetano lo empleamos para enfriar el chocolate fundido previamente y dar lugar a una trufa. Veamos cómo.
Este gas se encuentra en el interior de un aerosol presurizado (comprimido a presión superior a la presión atmosférica) y licuado (en estado líquido aunque en equilibrio con parte del tetrafluoroetano que sigue en estado gaseoso). Al accionarse el mecanismo de salida del aerosol, el tetrafluoroetano sale al exterior donde la presión es la atmosférica, inferior a la existente en el interior del aerosol.
 Debido a esa diferencia de presiones entre el interior y el exterior del aerosol, el tetrafluoroetano se vaporiza al salir fuera del recipiente absorbiendo calor del medio que lo rodea. Este hecho provoca una reducción de la temperatura tanto del medio externo como de cualquier objeto con el que entra en contacto el tetrafluoroetano, como es el caso del chocolate. Así, este se solidifica debido a esa bajada de temperatura dando lugar a una maravillosa trufa porosa de caprichosas formas gracias al «arte» de Xabi para moldear el chocolate.
Debido a esa diferencia de presiones entre el interior y el exterior del aerosol, el tetrafluoroetano se vaporiza al salir fuera del recipiente absorbiendo calor del medio que lo rodea. Este hecho provoca una reducción de la temperatura tanto del medio externo como de cualquier objeto con el que entra en contacto el tetrafluoroetano, como es el caso del chocolate. Así, este se solidifica debido a esa bajada de temperatura dando lugar a una maravillosa trufa porosa de caprichosas formas gracias al «arte» de Xabi para moldear el chocolate.
Pero cuando yo ya estaba dispuesto a comerme la trufa al tetrafluoroetano mi compi me lo impidió…quedaba el punto final. Como broche a esta deliciosa delicatessen se sacó de la manga el oro alimentario. En realidad les estoy hablando de partículas muy pequeñas de oro dispersas dentro de un gas presurizado y licuado presente en otro aerosol. Al igual que les expliqué anteriormente para el caso del tetrafluoroetano, al abrir la espita del aerosol sale el metano y, en esta ocasión, arrastra las partículas de oro que impregnan la trufa.
¿Pero este oro se puede comer? Por supuesto. El oro alimentario no es ni más ni menos que el aditivo E-175, un colorante que ha pasado todos los controles físico-químicos y sanitarios que establece la Unión Europea. Eso sí, este aditivo que fue muy utilizado en la Europa Medieval para decorar alimentos y bebidas como símbolo de riqueza y poderío, no proporciona propiedades nutricionales.
¿Pero es oro de verdad? Claro que sí, y lo podemos encontrar en polvo, en capas, en copos, en cuadraditos, en láminas, en filamentos… En el siguiente video pueden ver el proceso de elaboración del oro alimentario.
Acabo. Espero que les haya gustado esta explicación científica que se esconde detrás de las trufa doradas al tetrafluoroetano. Sí, ya lo sé. Con el “rollo de la divulgación científica” me estoy poniendo las botas en Órbita Laika… es lo que hay.

Trufa dorada al tetrafluoroetano (Fuente; http://xabiergutierrezcocinero.com)
Jose
Nota: Una vez más me gustaría recordar que los videos de “Ciencia en la cocina” han sido realizados por K2000 para la Cátedra de Cultura Científica de la UPV/EHU y cuentan con el asesoramiento científico de Yanko Iruín , responsable de una de mis bitácoras de referencia: El blog del Búho.
* Aqui pueden ver el resto de posts de la serie «Ciencia en la cocina»:
2.- Frutas pomposas bajo un volcán de caseínas
3.- El carbón dulce de los Reyes Magos
4.- Postre fractal con hidromiel
5.- Ensalada de chile camuflado con carragenano y ácido carmínico




El diccionario de Android me jugó una pequeña pasada y me cambió reciente, por recipiente, cuando tenía que haber aparecido este último en el texto enviado anteriormente. Saludos
Tres cosas:
– ¿No podría usarse aire comprimido en lugar de tetrafluorocarbono? Si el tema de que se enfríe es por la pérdida repentina de presión, también pasaría con aire, ¿no?
– ¿El metano no apesta?
– ¿No es inmoral usar oro para alimentación? No aporta nutriente alguno ni tampoco sabor, solo estatus y postureo. ¿Se acaba la cena encendiendo un puro con un billete de 20€?
Oiga joven, ¿no necesitan un probador de manduca?, la gente del norte nos adaptamos a cualquier tipo de comida 🙂
» el aditivo E-175, un colorante»….Esto me llamó la atención, pero por cierto que todas las explicaciones dadas en este post, andan al pelo para disfrutar doblemente el vídeo!
Reblogueó esto en Pitublog.
Pingback: Lo Mejor de la Semana (25-31 de enero) | Hablando de Ciencia | Artículos
Pingback: Resumen Scientia [Enero 2015] | SCIENTIA
Pingback: Ciencia en la Cocina (VII): La aparente contradicción entre los helados eutécticos y el deshielo de carreteras | SCIENTIA
Pingback: Ciencia en la cocina: Trufa dorada al tetrafluoretano | Ciencia en la cocina | Cuaderno de Cultura Científica
Pingback: Ciencia en la Cocina (VIII): Crómlech de mandioca al cianuro de hidrógeno | SCIENTIA
Pingback: La “Ciencia en la Cocina” de Órbita Laika explicada en 12 vídeos | SCIENTIA
Pingback: Un chocolate de cristal con textura de terciopelo | Ciencia para llevar
Pingback: Un chocolate de cristal con textura de terciopelo | Blog JEDA Granada
Pingback: Ciencia en la cocina (VI): Trufas doradas al te...